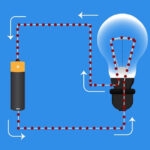
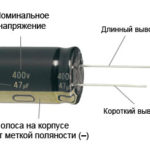
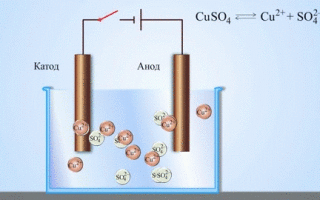
Pogosto se pojavi težava pri določanju, katera od elektrod je katoda in katera anoda. Najprej morate razumeti pogoje.
Vsebina
Koncept katode in anode - preprosta razlaga
V kompleksnih snoveh so elektroni neenakomerno porazdeljeni med atome v spojinah. Zaradi interakcije se delci premikajo iz atoma ene snovi v atom druge. Reakcija se imenuje redoks. Izguba elektronov se imenuje oksidacija, element, ki oddaja elektrone, pa se imenuje redukcijsko sredstvo.
Dodajanje elektronov se imenuje redukcija, sprejemni element v tem procesu je oksidant. Prenos elektronov iz redukcijskega sredstva v oksidacijsko sredstvo lahko poteka po zunanjem vezju, nato pa se lahko uporablja kot vir električne energije.Naprave, v katerih se energija kemične reakcije pretvori v električno energijo, imenujemo galvanske celice.
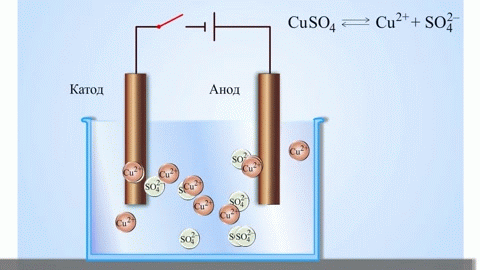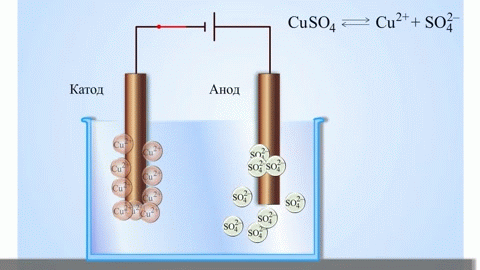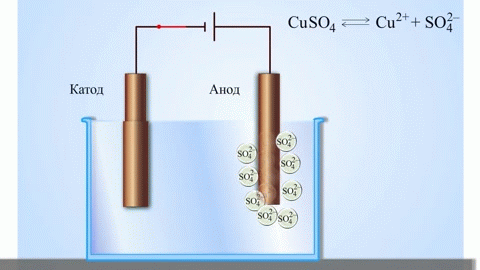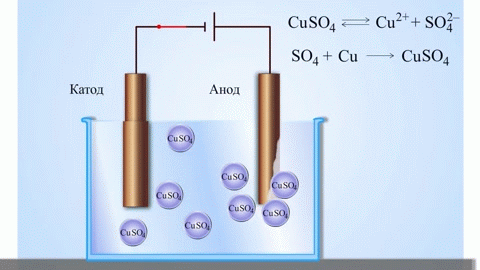
Najenostavnejši klasičen primer galvanskega elementa sta dve plošči iz različnih kovin in potopljeni v raztopino elektrolita. V takem sistemu se na eni kovini pojavi oksidacija, na drugi pa redukcija.
POMEMBNO! Elektroda, na kateri pride do oksidacije, se imenuje anoda. Elektroda, na kateri poteka redukcija, je katoda.
Iz šolskih učbenikov kemije je znan primer bakreno-cinkovega galvanskega elementa, ki deluje zaradi energije reakcije med cinkom in bakrovim sulfatom. V napravi Jacobi-Daniel se bakrena plošča postavi v raztopino bakrovega sulfata (bakrena elektroda), cinkova plošča je potopljena v raztopino cinkovega sulfata (cinkova elektroda). Cinkova elektroda oddaja katione v raztopino in v njej ustvarja presežek pozitivnega naboja, na bakreni elektrodi pa se raztopina izčrpa s kationi, tukaj je raztopina negativno nabita.
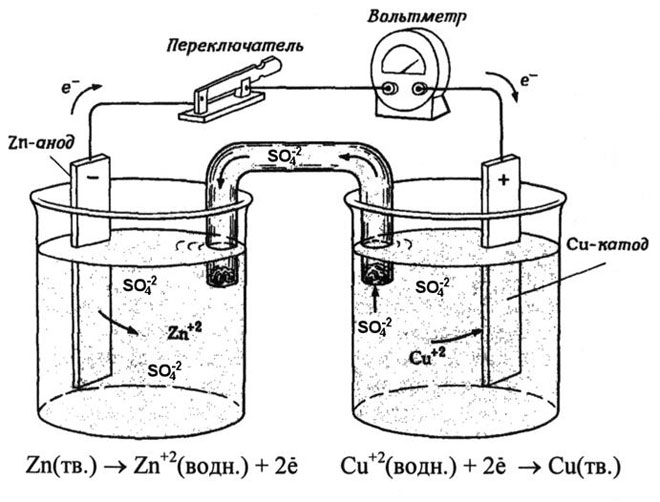
Zapiranje zunanjega vezja povzroči, da elektroni tečejo od cinkove elektrode do bakrene elektrode. Ravnotežna razmerja na faznih mejah so prekinjena. Poteka oksidacijsko-redukcijska reakcija.
Energija spontane kemične reakcije se pretvori v električno energijo.
Če kemično reakcijo izzove zunanja energija električnega toka, poteka proces, imenovan elektroliza. Procesi, ki se pojavljajo med elektrolizo, so obratni od procesov, ki se pojavljajo med delovanjem galvanskega elementa.
POZOR! Elektroda, kjer poteka redukcija, se imenuje tudi katoda, vendar je pri elektrolizi negativno nabita, medtem ko je anoda pozitivno.
Uporaba v elektrokemiji
Anode in katode sodelujejo v številnih kemičnih reakcijah:
- elektroliza;
- Elektroekstrakcija;
- galvanizacija;
- Elektrotip.
Kovine pridobivamo z elektrolizo staljenih spojin in vodnih raztopin, kovine čistimo od nečistoč in ekstrahiramo dragocene sestavine (elektrolitsko rafiniranje). Plošče so ulite iz kovine, ki jo je treba očistiti. Postavljeni so kot anode v elektrolizer. Pod vplivom električnega toka se kovina raztaplja. Njegovi kationi gredo v raztopino in se izpraznijo na katodi ter tvorijo usedlino čiste kovine. Nečistoče, vsebovane v originalni neočiščeni kovinski plošči, ostanejo netopne kot anodno blato ali pa preidejo v elektrolit, kjer se odstranijo. Baker, nikelj, svinec, zlato, srebro, kositer so podvrženi elektrolitskemu rafiniranju.
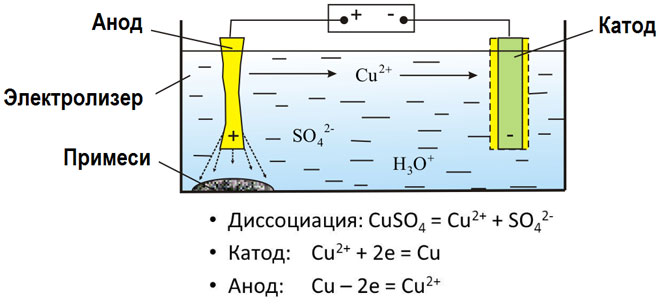
Elektroekstrakcija je postopek ločevanja kovine iz raztopine med elektrolizo. Da bi kovina šla v raztopino, jo obdelamo s posebnimi reagenti. Med postopkom se na katodi obori kovina visoke čistosti. Tako se pridobiva cink, baker, kadmij.
Da bi se izognili koroziji, dali moč, okrasili izdelek, je površina ene kovine prekrita s plastjo druge. Ta postopek se imenuje galvanizacija.

Galvanizacija je postopek pridobivanja kovinskih kopij iz razsutih predmetov z elektrodepozicijo kovine.

Uporaba v vakuumskih elektronskih napravah
Načelo delovanja katode in anode v vakuumski napravi lahko dokažemo z elektronsko svetilko.Izgleda kot hermetično zaprta posoda s kovinskimi deli v notranjosti. Naprava se uporablja za popravljanje, generiranje in pretvarjanje električnih signalov. Glede na število elektrod so:
- diode;
- triode;
- tetrode;
- pentode itd.
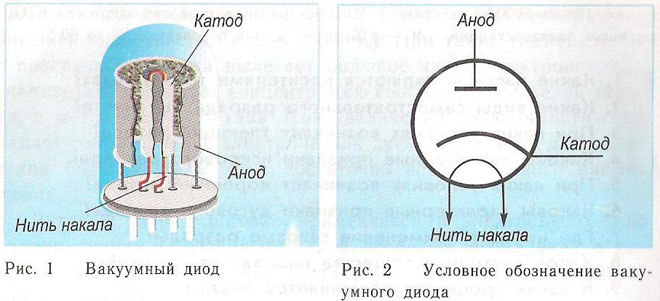
Dioda je vakuumska naprava z dvema elektrodama, katodo in anodo. Katoda je povezana z negativnim polom vira energije, anoda - s pozitivnim. Namen katode je oddajati elektrone, ko se segreje z električnim tokom na določeno temperaturo. Oddani elektroni ustvarijo prostorski naboj med katodo in anodo. Najhitrejši elektroni hitijo k anodi in premagajo negativno potencialno pregrado vesoljskega naboja. Anoda sprejme te delce. V zunanjem vezju nastane anodni tok. Elektronski tok nadzirajo dodatne elektrode z uporabo električnega potenciala nanje. S pomočjo diod se izmenični tok pretvori v enosmerni.
Uporaba v elektroniki
Danes se uporabljajo polprevodniške vrste diod.
V elektroniki se pogosto uporablja lastnost diod, da prehajajo tok v smeri naprej in ne v nasprotni smeri.
Delovanje LED temelji na lastnosti polprevodniških kristalov, da svetijo, ko tok prehaja skozi p-n spoj v smeri naprej.
Galvanski enosmerni viri - baterije
Kemični viri električnega toka, v katerih potekajo reverzibilne reakcije, se imenujejo baterije: polnijo se in uporabljajo večkrat.

Med delovanjem svinčene baterije pride do redoks reakcije.Kovinski svinec oksidira, daruje svoje elektrone, reducira svinčev dioksid, ki sprejema elektrone. Svinčena kovina v bateriji je anoda in je negativno nabita. Svinčev dioksid je katoda in je pozitivno nabit.
Ko se baterija izprazni, se porabljajo snovi katode in anode ter njun elektrolit, žveplova kislina. Za polnjenje baterije je priključen na vir toka (plus na plus, minus na minus). Smer toka je zdaj obratna od tiste, ki je bila, ko je bila baterija izpraznjena. Elektrokemični procesi na elektrodah so »obrnjeni«. Zdaj svinčena elektroda postane katoda, na njej poteka redukcijski proces, svinčev dioksid pa postane anoda, pri čemer poteka postopek oksidacije. Baterija ponovno ustvari snovi, potrebne za njeno delovanje.
Zakaj prihaja do zmede?
Težava nastane zaradi dejstva, da določenega znaka naboja ni mogoče trdno pritrditi na anodo ali katodo. Pogosto je katoda pozitivno nabita elektroda, anoda pa negativna. Pogosto, vendar ne vedno. Vse je odvisno od procesa, ki poteka na elektrodi.
POZOR! Del, ki je nameščen v elektrolit, je lahko tako anoda kot katoda. Vse je odvisno od namena postopka: nanjo morate nanesti še eno plast kovine ali jo odstraniti.
Kako prepoznati anodo in katodo
V elektrokemiji je anoda elektroda, na kateri potekajo oksidacijski procesi, katoda je elektroda, kjer pride do redukcije.
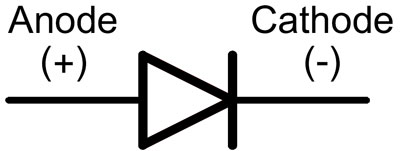
V diodi se pipe imenujemo anoda in katoda. Tok bo tekel skozi diodo, če je anodna pipa priključena na "plus", "katodna" pipa - na "minus".
Za novo LED z nerezanimi kontakti se anoda in katoda vizualno določita po dolžini. Katoda je krajša.

Če so kontakti odrezani, bo pomagala baterija, ki je nanje pritrjena. Svetloba se bo pojavila, ko se polaritete ujemajo.
Znak anode in katode
V elektrokemiji je pravilneje govoriti ne o znakih nabojev elektrod, temveč o procesih, ki potekajo na njih. Reakcija redukcije poteka na katodi, oksidacijska reakcija pa na anodi.
V elektrotehniki je za pretok toka katoda povezana z negativnim polom tokovnega vira, anoda s pozitivnim.
Podobni članki: